

�l���r�g��2021-10-25���ٷ�����̎��QՓ���g�[��1��
ժ Ҫ�� ժҪ:��̽����Q��ˮ̎��S������ˮ�˜ʲ�����߶�������̎�����g�y�}�������˰�����Ȟ�10mg/L��ģ�M�Uˮ��������������Ȼ��ʯ���������������M��̎����Ч�����о���Ӱ�̎��Ч������Ҫ���أ���̽ӑ��ȥ���C�����Y����������Ȼ��ʯ���͝�Ȱ��������@����ȥ
����ժҪ:��̽����Q��ˮ̎��S������ˮ�˜ʲ�����߶�������̎�����g�y�}�������˰�����Ȟ�10mg/L��ģ�M�Uˮ��������������Ȼ��ʯ���������������M��̎����Ч�����о���Ӱ�̎��Ч������Ҫ���أ���̽ӑ��ȥ���C�����Y����������Ȼ��ʯ���͝�Ȱ��������@����ȥ��Ч��;pH�������r�g��������Ͷ��������ʯ������������ȥ���ʾ���Ӱ푡���pH7.0����ʯͶ������12g/L��������0.6��0.9mm�������r�g��60min�ėl���£���ʯ��������ȥ�����_��80.38%��ʣ�ఱ��С��2.0mg/L����ˮ���_��GB3838—2002�ر�ˮ��˜ʡ�ԓ��ˇ����ˮ̎��S���|�о�����Ҫ�đ��Ãrֵ��
�����P�I�~:��Ȼ��ʯ;�͝�Ȱ���;�x��������;��ˮ�S���|
�������҇�ˮ�h�����o�Č��`�У���������Ҫ����Ⱦ�����ָ�ˣ�������oՓ����Ȼ�h��߀�����w����������ɲ��ɺ�ҕ�Ă��������������ˮ�w���I�B������Ҫ���أ�����һ���l�������D���Ɂ������}���M�����w������l���w�cθ�ϵK�����FѪ�t���װY�ȣ��^�ߵā������}߀��Ӱ����w���S����A�����ա���ˣ�̎��Uˮ���^���İ������ڭh���c����ʮ�ֱ�Ҫ��
����Ŀǰ���ڰ����Uˮ��̎����õ�������������ڶ���̎����ďUˮ��������ȵ͡�̼���ױ���ʧ�⣬����y���^�m�������̎�������ǣ����W��������Ĥ���x�������c���ȷ����������ȑ��ÏV��[1]����ȶ��ԣ���Ȼ��ʯ����һ�N�^���r���õ������������ڏUˮ�еİ������^�����x����������[2]����̎�������Uˮ�������x�F�A�γ��ڭh�����]�����Uˮ�ŷ�����˸��ߵ�ˮ�|Ҫ����Ҫ�M��ر����ˮ�˜��������ߣ��������y̎�����ǏUˮ�еİ��������ڴˣ��о���Ȼ��ʯ���͝�Ȱ����Uˮ��ȥ��Ч����������Ӱ������Լ�ȥ���C���M��̽ӑ������̽����ˮ���̎���ĸ�Ч��Q����������Ҫ���x��
����1����
����1.1���ϡ�ԇ�����x��
����������õ�����Ȼ��ʯ���Խ��Kʡ����ҾGɫ�w�����w��ͨ�^��ĥ�ͺY�ֵõ�����������0.6��0.9��0.9��2��2��3mm����Ȼ��ʯ����ʯ��ȥ�x��ˮ���͛_ϴ��ֱ���_ϴˮ���ٜ��ᣬ��ȥ��������ɳ��ˮ���Ԛ�����Ȳ������|������(60±5)���º��24h��
�����⻯�����⻯⛡��������c���}�ᡢ��ʯ����c��NH4Cl�ȣ��������۷�����;���������Һ����MilliporeMilli-Q����ˮϵ�y���ơ�
����752N����-��Ҋ�ֹ���Ӌ(��10mm��ɫ��);HJ-6A�����@�ش���������;DHG-9070B������늟��ع��L������;TG328B��W������ƽ;FE28pHӋ��
����1.2�͝�Ȱ����Uˮ�����Ƽ��y������
�������]���������ˮ̎��S��Ⱦ���ŷŘ˜ʡ�(GB18918—2002)��һ��A�˜ʰ�����������5��8mg/L������������15mg/L���������NH4Cl���Ɲ�Ȟ�10mg/L�İ���ģ�M�Uˮ���ü{��ԇ���ֹ��ȷ��y��������ȡ�
����1.3����
�������ö����Γu����ʎ���M�з�ʯ����������������250mL�F��ƿ�м���100mLһ����ȵ�NH4Cl��Һ�Ͷ����ķ�ʯ�w��������180r/min�ĺ����ʎ���з���һ���r�g��y��ʣ�ఱ����ȣ���Ӌ��������ȥ���ʡ�ͨ�^��׃��ʯ������pH����ʯ�����������r�g�����ش_����������l�������о����������ԡ�ÿ�M����O��3��ƽ�Иӱ���
����2�Y���cӑՓ
����2.1��Ȼ��ʯ�����Uˮ�е�����Ӱ����ط���
����2.1.1pH�������^�̵�Ӱ�
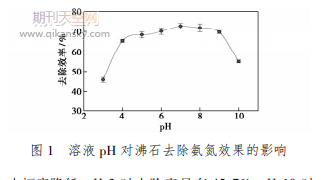
����ȡ100mL��ʼ��Ȟ�10mg/L��NH4Cl��Һ���O���ضȞ�25�棬������Ͷ������1g�������r�g12h����0.01mol/L�}����Һ��0.01mol/L�������c��Һ�{��ˮ��pH��3��10������pH����ʯȥ������Ч����Ӱ푣��Y��Ҋ�D1��
�����Y��������pH��3��7֮�g�r����ʯ��������ȥ������u���ߣ�����pH��7�rȥ��Ч����ã��_��72.7%����pH������5��9�r����ʯȥ������Ч�ʶ��ɱ�����70%���ң��^����^�A�h����ȥ��Ч�ʴ���Ƚ��ͣ�pH3�rȥ����ֻ��45.7%��pH10�rȥ����ֻ��55.1%���@�����ډA�ԗl���·�ʯ�l�������ܽ�[3]�Լ�NH+4���D���鰱���Ӵ�������Һ�У������ڱ�����[4]�����ڵ�pH�h���£���Һ�е�NH+4����cH+���Z��ʯ���x�ӽ��Qλ�c���@�N�����ӄ�ʹ�ð�����ȥ���ʽ���[5]��
����2.1.2��ʯͶ����������Ч����Ӱ�
����ȡ100mL��ʼ��Ȟ�10mg/L��NH4Cl��Һ���O���ضȞ�25�棬�����r�g12h����ҺpH7����ʯ������0.6��0.9mm����ʯͶ�����քe��0.05��0.1��0.2��0.4��0.6��0.8��1.2��1.6��2.0g������������Ͷ��������ʯȥ������Ч����Ӱ푣��Y��Ҋ�D2��
�������P֪�R���]����ˮ̎�����̎��u�Q��ô�x���l��Փ��
�����Y����������ʯȥ��������Ч���S�����������������Ӷ���u��ߣ���ʯͶ������0.5g/L���ӵ�20g/L�r��������ȥ���ʏ�8.50%��ߵ�93.66%���@�������������ṩ�˸���ĽY��λ�c��ʹNH+4�����םB������λ�c���Ķ������ȥ���ʡ��ĈD2߀�ɿ�������ʯͶ�������^12g/L��ȥ������������ƽ�����^�m����������������ȥ��Ч�ʵ���߷��ȿɺ��Բ�Ӌ���@������������Һ�Ў����е��x�Ӷ��c�������Y�ϣ��Լ��Y�����������ϵ��x���c��Һ��δ�����յ��x��֮�g������ƽ��[4]�������^�ߵĹ�Һ�����γ��˾ۼ��w�����w������������[6]�����]���ɱ���ȥ��Ч�����x���ʯ�����mͶ������12g/L��
����2.1.3�����Լ����|�r�g������Ч����Ӱ�
����ȡ100mL��ʼ��Ȟ�10mg/L��NH4Cl��Һ���O���ضȞ�25�棬������Ͷ������1g���O�������r�g�քe��10��20��30��40��50��60��90��120��180��240��300min�����������քe��0.6��0.9��0.9��2��2��3mm�ķ�ʯ�w��������ȥ��Ч����Ӱ푣��Y��Ҋ�D3��
�����Y��������������ȥ�����S��ʯ�����ĜpС�ͽ��|�r�g�����Ӷ����ӡ���ʯ������2��3mm�pС��0.6��0.9mm��������ȥ��Ч�ʏ�56%������71%���@�����ڷ�ʯ����ԽС�ȱ���eԽ���^��ıȱ���e�����M����������ʹ�÷�ʯ�������x���c��Һ�е���x���װl�����Q[7]�����⣬�����w��������ʯȥ��������һ���������ٵ��^��[8]����ǰ60minȥ���ʾ��_����60%���ң�60��120minȥ�������L��u�p������120min���������_��ƽ�⣬�˺�ͬ������ʯ��������ȥ����׃�������@�����Dz�ͬ�����ķ�ʯ�_������ƽ��ĕr�g��ͬ��������0.6��0.9��0.9��2��2��3mm�ķ�ʯ�w����������r�g�քe��88��117��184min��С������ʯ��������r�g���@�s�̣���0.6��0.9mm�ķ�ʯ50minȥ���ʼ����_��56%���ҡ�
����2.2���������W����
�������о���ʯ�������������C�����u���������ܣ��������Y������Lagergren��һ�A�����W��Ho�ζ��A�����Wģ�ͺͷ��ӃȔUɢģ�͌�����^���M��������
����2.3��Ȼ��ʯ�����͝�Ȱ����^�̷���
������ʯ�����͝�Ȱ�����Һ��һ�Nǰ�ڿ����M�С����������ٶȜp����������u�_������ƽ����^�̣�������ԽС�_������ƽ��Խ�졣�@������ǰ�������A�Σ���ʯ��������λ�c�^�࣬NH+4���ٓ�ռλ�c�����������M�С��S������λ�c�Ĝp�������^����u�p��ֱ���_������ƽ�⡣�����������W�о��У��ζ��A�����Wģ�ͱȂ�һ�A�����Wģ���Ӝʴ_�ؔM���ˌ��������w���ȔUɢģ�͔M���У��ɶβ��B�m�ĔM���������Ա�����ʯ�������������漰�������������ӃȔUɢ�ɂ��A�Σ��@�f�����ӃȔUɢ����Ψһ�����ʿ��Ʋ��E���Y�ψD6�͈D3���Կ�������ǰ60min�ȷ�ʯ��������������Ҫ��߅��ӃȔUɢ[13]����������������הUɢ[14]���˺��������Ҫ�����ӃȔUɢ��С�הUɢ�M�С���������^���У��_ʼ�A�ΰl�����ٔUɢ������ڃȱ���l���dz������ĔUɢ���@�c֮ǰ�W�߂����о��Y��һ��[15-16]��
����3�YՓ
������ʯȥ���͝�Ȱ����Uˮ���о���Ҫ�YՓ����:
����(1)��ʯ����������һ��������Ч�������������x���ԡ�
����(2)��ҺpH�������������������r�g����������Ӱ�����Ч�������أ�����������Խ������ԽСȥ����Խ�ߣ������^��ԽѸ�١���ʯ�����ԗl��������������Ч���^�ߡ���ʯ��pH7.0��Ͷ������12g/L��������0.6��0.9mm�������r�g��60min�ėl����������ȥ�����_��80.38%���M��ر����ˮ�˜�Ҫ��
����(3)��Ȃ�һ�Aģ�ͣ��ζ��A�����Wģ�Ϳ��Ը��ʴ_��������ʯȥ�������Ą����WҎ�ɣ��f�������^���Ի��W��������;���w���ȔUɢģ�̓H�m���������ɷN�����^�̵�ijһ�A�Σ�������ʯ��������������ǰ60min����Ҫ��߅��ӃȔUɢ���˺��������Ҫ�����ӃȔUɢ��С�הUɢ�M�С�——Փ�����ߣ��Z�ǽܣ�����*����t�G������
SCISSCIAHCI